UNIDAD III
INTRODUCCION
El carbono
es un elemento químico de numero atómico 6 y símbolo C. Es
solido a temperatura ambiente. Dependiendo de las condiciones
de formación, puede encontrarse en la naturaleza en distintas
formas alotrópicas, carbono amorfo y cristalino en forma de grafito o
diamante. Es el pilar básico de la química orgánica; se
conocen cerca de 16 millones de compuestos de carbono aumentando este
numero en unos 500.000 compuestos por año, y forma parte de todos los
seres vivos conocidos. Forma el 0,2% de la corteza terrestre.
El
carbono puro existe bajo formas alotrópicas como sólidos, cristalinos
naturales y artificiales,y en forma impura como solidos amorfos
naturales y artificiales.
La química orgánica define la vida. Así como hay millones de diferentes tipos de organismos vivos en este planeta, hay millones de moléculas orgánicas diferentes,
cada una
con propiedades químicas y físicas diferentes.
Hay químicos orgánicos que son parte del pelo, piel, uñas, etc. La
diversidad de químicos orgánicos tiene su origen en la versatilidad
del átomo de carbono.
El cabono tiene numero atomico 6 con 2 electrones interiores
y 4 exteriores haciendo que el atomo pueda en lazarse con
atomos mas formando moleculas como hidrocarburos .
ISOMERIA La isomería consiste en que dos o más sustancias que responden a la misma fórmula molecular presentan propiedades químicas y/o físicas distintas.
Tipos de isomería
Isomería estructural o plana
La isomería estructural o plana se debe a diferencias de estructura y puede explicarse mediante fórmulas planas.
a) Isomería de cadena
Es la que presentan las sustancias cuyas fórmulas estructurales difieren únicamente en la disposición de los átomos de carbono en el esqueleto carbonado
CH3-C=CH-CH2-CH2-CH3
I
CH3
2metil-2hexeno
b) Isomería de posición
Es la que presentan sustancias cuyas fórmulas estructurales difieren únicamente en la situación de su grupo funcional sobre el esqueleto carbonado.
CH2=CH--CH2--CH3 ------------------------------>1-buteno C4H8
c) Isomería de función
Es la que presentan sustancias que con la misma fórmula molecular presentan distinto grupo funcional
CH3-CH2-CH2OH Y CH3-CH2-O-CH3
Estereoisomería: Isomería geométrica
La estereoisomería la presentan sustancias que con la misma estructura tienen una diferente distribución espacial de sus átomos.
Una de las formas de estereoisomería es la isomería geométrica. La isomería geométrica desde un punto de vista mecánico, se debe en general a que no es posible la rotación libre alrededor del eje del doble enlace. Es característica de sustancias que presentan un doble enlace carbono-carbono
Para que pueda darse en los compuestos con doble enlace, es preciso que los sustituyentes sobre cada uno de los carbonos implicados en el doble enlace sean distintos. Es decir, que ninguno de los carbonos implicados en el doble enlace tenga los dos sustituyentes iguales.
Las distribuciones espaciales posibles para una sustancia que con un doble enlace son:
Forma cis; en ella los sustituyentes iguales de los dos átomos de carbono afectados por el doble enlace se encuentran situados en una misma región del espacio con respecto al plano que contiene al doble enlace carbono-carbono.
Forma trans; en ella los sustituyentes iguales de los dos átomos de carbono afectados por el doble enlace se encuentran situados en distinta región del espacio con respecto al plano que contiene al doble enlace carbono-carbono.
Estereoisomería. Isomería óptica
Existen sustancias que al ser atravesadas por luz polarizada plana producen un giro del plano de vibración de la luz. Se dice que estas sustancias presentan actividad óptica.
Se llaman sustancias dextrógiras las que al ser atravesadas por una luz polarizada plana giran el plano de polarización hacia la derecha (según un observador que reciba la luz frontalmente).
Se llaman sustancias levógiras las que al ser atravesadas por una luz polarizada plana giran el plano de polarización hacia la izquierda (según un observador que reciba la luz frontalmente).
La causa de la actividad óptica radica en la asimetría molecular. En química orgánica la principal causa de asimetría molecular es la presencia en la molécula de algún átomo de carbono asimétrico. El átomo de carbono asimétrico se caracteriza por estar unido a cuatro grupos diferentes. Se acostumbra a señalar los carbonos asimétricos con un asterisco cuando se quiere poner de manifiesto su carácter de carbonos asimétricos:
En el caso de una molécula con un sólo átomo de carbono asimétrico son posibles dos configuraciones distintas y tales que una cualquiera de ellas es la imagen especular de la otra. Estas configuraciones son recíprocamente enantiomorfas.
HIDROCARBUROS
Los hidrocarburos son compuestos organicos formados únicamente por atomos de carbono e hidrogeno. La estructura molecular consiste en un armazón de átomos de carbono a los que se unen los átomos de hidrógeno. Los hidrocarburos son los compuestos básicos de la quimica organica. Las cadenas de átomos de carbono pueden ser lineales o ramificadas y abiertas o cerradas. Los que tienen en su molécula otros elementos químicos (heteroatomos),se denominan hidrocarburos sustituidos.
Los hidrocarburos se pueden clasificar en dos tipos, que son alifaticos y aromaticos. Los alifáticos, a su vez se pueden clasificar en alcanos, alquenos y alquinos según los tipos de enlace que unen entre sí los átomos de carbono. Las formulas generales de los alcanos, alquenos y alquinos son CnH2n+2, CnH2n y CnH2n-2, respectivamente.
En la actualidad nos afecta los hidrocarburos tanto alos humanos y al ambiente ya que en nuestro cuerpo es grasa dificil de dijerir y en el ambiente son gases que degradan la capa de ozono O3 que al desbanecerse hara que los rayosultravioletas toquen la tierra calentandola mucha hasta que la tierra se quede sin vida.
Ejercicios
Adicionales Nomenclatura de Hidrocarburos.
1) En las
siguientes fórmulas, elige la cadena principal y nombra el compuesto:
a) CH3–CH (CH3) –CH2–CH (CH3) –CH2–CH3
b) (CH3–CH2)3–CH
c) CH3–CH2–C (CH3)3
d) CH3 –CH2 –CH(CH3) –CH2–CH(CH2 -CH3) –CH2–CH (CH3) -CH3
e) CH3 –CH= C (CH3) –CH2–CH(CH2 -CH3) –CH2–CH (CH3) -CH3
f) CH2= CH–C(CH3)2–CH = C(CH2 -CH3) –CH2–CH (CH3) -CH3
g) CH3 –CH2 –CH(CH3) –CH2–C =C–CH (CH3) -CH3
2) Escribe
las fórmulas semidesarrolladas de los compuestos dados y clasifica a cada uno:
a) Metil
benceno
b) 2,3-dimetil-2-hexeno
c) 2,4-dimetil-3,3,4-trietilheptano
d) 3-etil-1-pentino
e) 3-metil-2-propil-1,5-hexadieno
f) 4-metil-4-isopropil-2-octino
3) Nombra
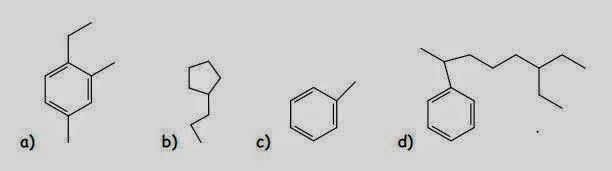
las sustancias representadas con los esquemas:
4) Escribe
las fórmulas semidesarrolladas de :
a) 3-etil-2-metilhexano
b) 4-metil-2-pentino
c) 3,4-dietil-1-heptenov
d) 3,5-dietil-2,4,6-trimetilheptano
e) 2,3-dimetil-1,4-heptadieno
f) metilciclohexano
g)3-metil-4-isopropil-1,6-octadiino
h) 2,3-dietil-2,6-dimetil-5-propildecano
5) Indica qué error se ha cometido al nombrar los siguientes compuestos:
a) 3-propilhexano
b) metilpropilmetano
c) 4-metilpentano
d) 3,3-dimetil-2,5-dietilheptano
RESPUESTAS
6)Nombra y clasifica cada uno de los compuestos cuyas fórmulas
semidesarrolladas se dan a continuación:
semidesarrolladas se dan a continuación:
e) CH3–CH (C3)–CH2-CH= CH-CH3
f) CH2= CH–CH2-CH (CH3) = CH (CH2-CH3)–CH3
g)CH3–C (CH2-CH3) (CH3)–C (CH3)2-C (CH3)2-CH3
h)CH2= CH–CH2-CH (CH3)–CH (CH2-CH2–CH)-CH
7)Clasifique los siguientes compuestos. Nómbrelos. Indique el tipo de
isomeríapresente entre ellos:
8)Formular los siguientes compuestos:
a) 3-metil-3-hepteno
b) 3,4-dimetil-3-hexeno
c) 2-metil-2-hexeno
d)2-metil-3-hexeno
e)2,4-dimetil-3-hepteno
f)2,4-dimetil-1,3-heptadieno
g)3-metil-1-octino
h)etilciclopentano
RESPUESTAS
1)
a) 2,4-dimetil hexano
b) Pentano
c) 2,2-dimetil butano
d) 4-etil-2,6-dimetil octano
e) 5-etil-3,7-dimetil-2-octeno
f) 5-etil-3,3,7-trimetil-1,4-octadieno
g) 2,6-dimetil-3-octino
2)

b) CH3 – C(CH3) = C(CH3) CH2 – CH2 – CH3
c) CH3 –CH (CH3) – CH (CH2 - CH3)2– CH (CH3) (CH2 - CH3) -CH2-CH2 – CH3
d) HC = C-CH (CH2-CH3)-CH2-CH3
e) CH2=C(CH2-CH2-CH3)-CH(CH3)-CH2-CH=CH2
f) CH3-C=C-C(CH3)(CH(CH3)2)-CH2-CH2-CH2-CH3
3)
a) Trans-6-isopropil-4-metil-1,7-nonadieno
b) (2-metil butil) benceno
c) 4,5,6,7-tetrametil-1-decino
d) 1-etil-2-metil ciclopentano
e) Trans-4,5-dimetil-6-propil-1,7-nonadieno
f) Cis-3-etil-2,4,5-trimetil-3-hepteno
g) 2,3-dimetil isopropilbenceno
4)
a) CH3-CH(CH3)-CH(CH2-CH3)-CH2-CH2-CH3
b) CH3-C=C-CH(CH3)-CH3
c) H2C=CH-CH(CH2-CH3)-CH(CH2-CH3)-CH2-CH2-CH3
d) CH3-CH(CH3)-CH(CH2-CH3)-CH(CH3)-CH(CH2-CH3)-CH(CH3)-CH3
e) H2C=C(CH3)-CH(CH3)-HC=CH-CH2-CH3
g) HC=C-CH(CH3)-CH(CH(CH3)2)-CH2-C=C-CH3
h) CH3-C(CH3)(CH2-CH3)-CH(CH2-CH3)-CH2-CH(CH2-CH2-CH3)-CH(CH3)-CH2-CH2-CH2-CH3
5)
a) el nombre correcto el propilhexano (no es necesario poner el 3 pues es la
única posición que puede tener el propil).
b) No se tomó la cadena más larga: el nombre correcto es metilbutano
c) La cadena está numerada al revés: 2-metilpentano
d) No respeta orden alfabético de grupos alquilo y hay una cadena más larga:
el nombre correcto es 6-etil-3,4,4-trimetiloctano.
6)
a) 2,4-dimetil etilbenceno
b) propilciclopentano
c) Tolueno
d) 6-etil-2-feniloctano
e) 5-metil-2-hexeno
f) 5-etil-4-metil-1,4-hexadieno
g) 2,2,3,3,4,4-hexametilhexano
h) 4,5-dimetil-1-octeno
7)
a) trans-3-metil-3-hexeno
b) 1-hepteno
c) metilciclohexano
d) o-xileno (o-dimetilbenceno)
e) 2-octino
f) cis-3-metil-3-hexeno
g) m-xileno
h) etilbenceno
8)
a) CH3-CH2-C(CH3)=CH-CH2-CH2-CH3
b) CH3-CH2-C(CH3)=C(CH3)-CH2-CH3
c) CH3-C(CH3)=CH-CH2-CH2-CH3
d) CH3-CH(CH3)-CH=CH-CH2-CH3
e) CH3-CH(CH3)-CH=C(CH3)-CH2-CH2-CH3
f) H2C=C(CH3)-CH=C(CH3)-CH2-CH2-CH3
g) HC=C-CH(CH3)-CH2-CH2-CH2-CH2-CH3¿Que usos tiene los hidrocarburos aromaticos?
En la actualidad, los principales usos de los compuestos aromáticos como productos puros son: la síntesis química de plásticos, caucho sintético, pinturas, pigmentos, explosivos, pesticidas, detergentes, perfumes y fármacos. También se utilizan, principalmente en forma de mezclas, como disolventes y como constituyentes, en proporción variable, de la gasolina.
Para que se de la aromaticidad deben cumplirse ciertas premisas, por elejemplo que los dobles enlaces resonantes de la molecula estan conjugados y que se den al menos dos formas resonantes equivalentes.
Se mostraran algunas imagenes sobre los usos que tiene los hidrocarburos aromaticos.
 |
| Disolvente con hidrocarburos Aromaticos |
 |
| Un perfume con hidrocarburos aromaticos. |
A continuacion se mostrara un mapa conceptual donde se demuestra el tipo de hidrocarburos que existen con sus caracteristicas y usos.
 |
| Hidrocarburos |
La importancia del uso moderado del petroleo.
Se debe de usar moderadamente ya que el petroleo tiene en relacion a todos los elementos y fenomenos que se generan a partir suyo, muchos de los cuales dan esencia a la vida moderna que solemos llevar.
El petroleo no es solo utilizado como combustible para todos los tipos de medios de locomocion (Locomocion es ir de un lugar a otro) si no que tambien es utilizado para la fabricacion de elementos y productos de todo tipo como el plastico.
Se debe de hacer un esfuerzo para llevar a cabo un uso moderado en el ambito de la locomocion ya que muchos usan el petroleo para sus autos en el cual alguno de ellos tienen fallas donde hace que expulsen mas humo.
Podemos señalar que el petroleo es importante en el ambito cuidado del medio ambiente ya que se lo considera como uno de los contaminantes mas fuertes que se pueden conocer. esto es asi debido a que se puede generar complicaciones serias en el medio ambiente por ejemplo cuando hay derrames o contaminaciones de recursos naturales como rios, terrenos, etc.
Propuesta para cuidar el medio ambiente:
Propuestas:
- No consumir agua embotellada
- Comprar comida que realmente se vaya a comer.
- Lavar la ropa a baja temperatura y evitar lavar con agua caliente.
- Tender la ropa en vez de usar la secadora.
- Utilizar productos de limpieza naturales y respetuosos con el medio ambiente y con nuestra salud.
- En vez de utilizar productos cosmeticos, usar cualidades de fitocosmeticos y formulas naturales que se puede preparar en la misma casa.
- In andando, en bicicleta o transporte publico siempre que sea posible o como minimo alguna vez a la semana.
- Comprar los libros de segunda mano, ir mas frecuentemente a la biblioteca, intercambiarlos con tu familia y amigos.
- Usar papel reciclado en la escuela o en tu oficina, no imprimir si no es realmente necesario, escoger las habitaciones con mas horas de liz, pintar paredes de un color claro, apagar el ordenador o la pantalla de este si estaras mucho rato sin usarlo.
- Evitar el consumismo.